Aufgabe 2)
a)-c) siehe Tabelle
Die Eizelmasse setzt sich aus den Massen von Protonen und Neutronen
zusammen:
meinzeln = k mp + (m-k) mn
Der Massendefekt ist die Differenz zwischen den Einzelmassen und der
tatsächlichen Masse:
Δm = meinzeln - m
Die Energie pro Nukleon ergibt sich aus der umgestellten
Einstein-Gleichung. Das Ergebnis muss noch durch die Massenzahl m
geteilt werden, um die Energie pro Nukleon zu bekommen.
Wpro Nukleon = Δm c2 /m
d)
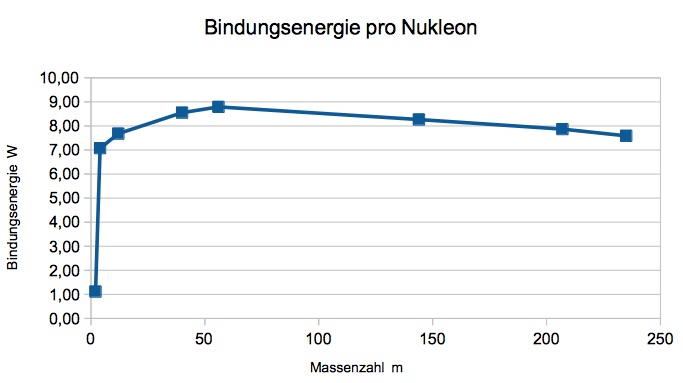
Die freigesetzte Energie pro Nukleon nimmt bis Eisen hin zu und sinkt
dann wieder. Damit können Kerne unter Eisen durch Kernfusion und Kerne
oberhalb Eisens durch Kernspaltung Energie freisetzen.
Besonders effektiv ist dabei die Kernfusion von Deuterium zu Helium.
|
| Element |
meinzeln in u |
Δm in u |
W/m in eV |
|
| D |
2,015941383 |
0,0024 |
1,11 |
|
| He |
4,031882766 |
0,0304 |
7,07 |
|
| C |
12,0956483 |
0,0989 |
7,68 |
|
| Ca |
40,31882766 |
0,367 |
8,55 |
|
| Fe |
56,44913562 |
0,528 |
8,79 |
|
| Ba |
154,1699947 |
1,278 |
8,27 |
|
| Pb |
208,6797848 |
1,748 |
7,87 |
|
| U |
236,9085179 |
1,914 |
7,59 |
|
 |
|
|