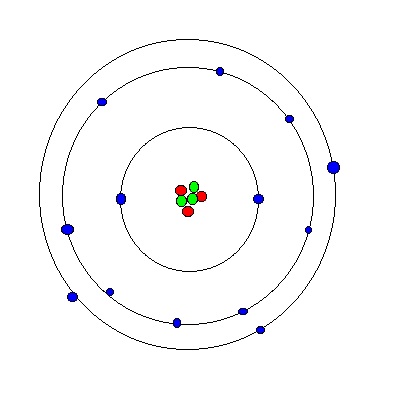
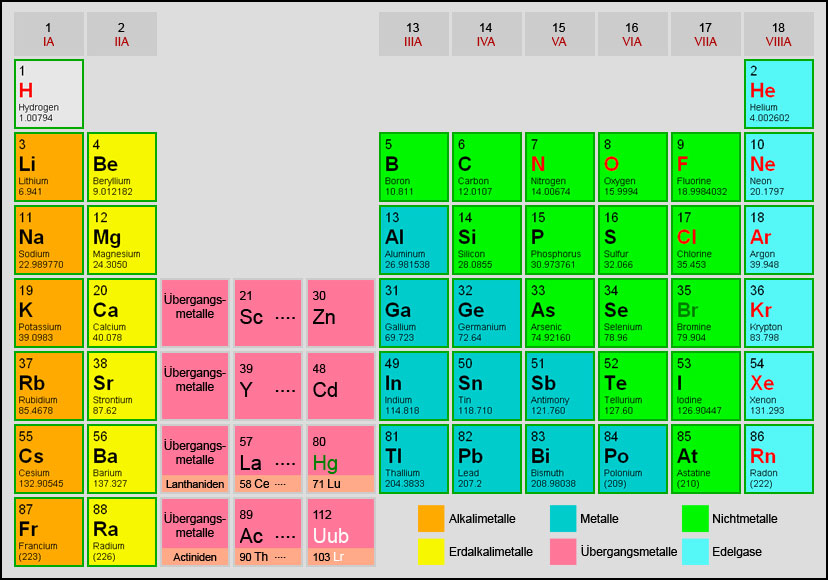
Ein Atom besteht aus drei Bestandteilen:
In der Atomhülle befinden sich die Elektronen mit einer Masse von 9,1 E-31kg und einer Ladung von -1,6 E-19 Coulomb.
Im Atomkern befinden sich Neutronen und Protonen.
Die Protonen haben eine Masse von 1,67 E-26 kg und eine Ladung von 1,6 E-19 C, d.h. die gleiche Ladung wie ein Elektron, allerdings im positiven Bereich.
Die Neutronen sitzen vereinfacht gesagt zwischen den Protonen im Kern und sorgen dafür, dass diese sich nicht aufgrund ihrer Ladung so stark abstoßen können, dass der Kern auseinanderfällt. Sie haben annähernd die gleiche Masse wie die Protonen, sind aber neutral geladen, d.h. die in ihnen enthaltenen Ladungen heben sich insgesamt auf.
| Teilchen | Masse | Ladung |
| Elektron | 9,1 E-31 kg | -1,6 E-19 C |
| Proton | 1,67 E-26 kg | +1,6 E-19 C |
| Neutron | 1,67 E-26 kg | 0 C |