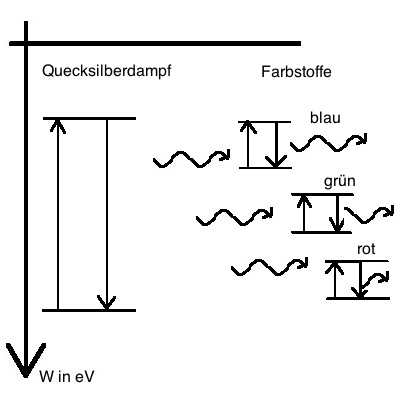
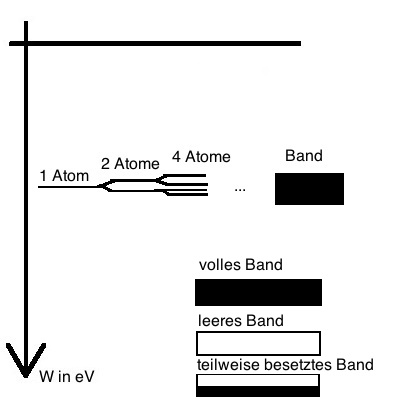
In einer mit Gas gefüllten Röhre werden freie Elektronen beschleunigt und stoßen dabei auf die Gasatome. Dort können sie bei ausreichender Energie Elektronen des Atoms auf höhere Energieniveaus heben.
Diese Elektronen können nun von höheren Energieniveaus auf tiefere fallen, sofern auf ihnen freie Plätze sind. Bei diesem Übergang kommt es zur Aussendung (Emission) von Licht.
Die Energie und damit auch die Wellenlänge und Frequenz des Lichtes entspricht damit der Energiedifferenz der beiden beteiligten Energieniveaus.
Ein Stoff kann in der Regel mehrere Lichtquanten bei entsprechenden Übergängen aussenden. Es entsteht ein sogenanntes Linienspektrum mit mehreren einzelnen Farblinien.
Anwendung findet dieses Prinzip in verschiedenfarbigen Leuchtröhren der Werbung und in den gelblichen Neondampflampen , die es z.T. noch im Straßenbild gibt. Dabei dominiert i.d.R. eine der Leuchtfarben.
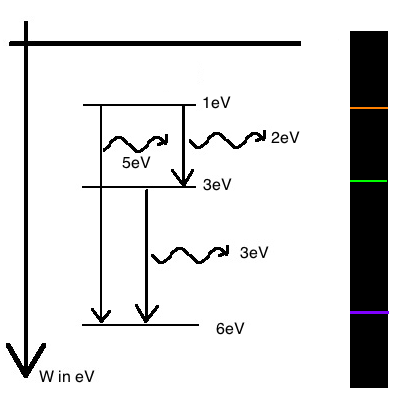 gif
gif
gif
gif